Хранение и прокалка электродов – что в премиум сегменте?
0
На сумму: 0 р.
Буквально на днях один из наших Клиентов, при заказе очередной порции сварочных материалов, в расстроенных чувствах поведал страшную историю:
В складском помещении предприятия протекла крыша, где были размещены паллеты с электродами, к несчастью они не были накрыты тентом. Трагедия пришлась на выходные, когда дежурила лишь охрана. Горький финал: ~200 кг промокших электродов, на части из них отвалилась обмазка.
Ситуация Клиента подтолкнула меня написать эту новость.
В прошлом месяце ESAB анонсировал новое оборудование для прокалки и хранения электродов.
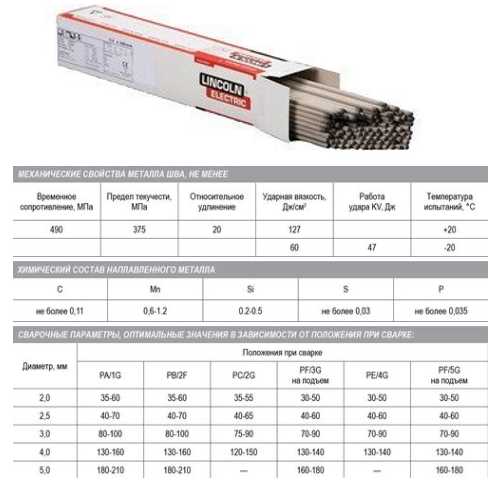
Давайте вспомним ликбез, когда требуется прокалка, в случае если ваши электроды не залил дождь:
Электроды при сварке могут давать поры, либо давать повышенное содержание диффузионно свободного водорода в наплавленном металле, если значения влажности при их хранении не соответствовали требованиям. Для возвращения им изначальных свойств, требуется прокалка.
Для возвращения им изначальных свойств, требуется прокалка.
- На ответственных участках покрытые электроды с основной обмазкой в обязательном порядке должны всякий раз подвергаться прокалке перед началом работ. Даже где-то видел плакаты с памятками.
- Электроды для сварки углеродистых сталей с кислым или рутиловым покрытием обычно прокалки не требуют.
- Электроды с целлюлозным покрытием прокаливать не рекомендуется.
Электроды прокаливаются без упаковки.
Электроды не рекомендуется прокаливать более трех раз.
Решения для прокалки и хранения электродов от ESAB
Что же подготовил ЭСАБ? Целых 2 линейки оборудования для прокалки электродов.
PSE – Portable Storage Electrode
Из аббривиатуры сразу выделяем особенность – портативные контейнеры для хранения электродов.
Оборудование для прокалки электродов ESAB PSE 5:
- Вместимость – 5 кг;
- Температура хранения 130°C.

Варианты PSE 10 и PSE 24:
Главная отличительная функциональность моделей от младшей это ручной термостат.
- Вместимость – 10 кг и 24 кг;
- Диапазон температуры хранения 60 – 200°C;
- Термостат.
Обзоры и практика применения оборудования,
инсайды производителей, новости!
Читайте бесплатно эксклюзивные материалы нашего блога.
Знания в 2021 году самый ценный из ресурсов!
Далее тяжелая гвардия. Аббривиатура SDE обозначает “Stationary Drying Electrode” – стационарная прокалка электродов.
Стационарные модели прокалки электродов ESAB SDE 50, SDE 100, SDE 250 и SDE 250 (380B) различаются лишь объемом контейнера и тем, что последняя модель работает от трехфазной сети 380В.
- Цифровой термостат с широким диапазоном регулировок температуры хранения;
- После прокалки температура автоматически опускается до рекомендованной температуры хранения в 130°C;
- Диапазон температуры прокалки 0-400°C.

С ценами можете ознакомиться в каталоге оборудования для прокалки и хранения электродов от ESAB.
А какими способами вы храните и прокалываете электроды? Какое оборудование используете?
Пишите в комментариях.Дмитрий Ягольник
Эксперт по сварочному оборудованию
Теги
- Новости
Спасибо за подписку!
Режимы прокалки электродов
Марка электрода | Режимы прокладки | |
Температура, °С | Продолжительность, ч | |
ЦЛ-39, ТМЛ-1У, ЦУ-2ХМ, ТМЛ-ЗУ, ЦЛ-20, ЦЛ-45. | 380 ± 20 | 2,0+ 0,5 |
ЭА-400/10У,
ЭА-400/10Т, ЦТ-26, ЦТ-26М, ЦТ-15, ЦТ-15К. | 220 ± 20 | 1,0 + 0,5 |
Примечание. Прокалка электродов может производиться не более трех раз. Если электроды после трех прокалок показали неудовлетворительные сварочно-технологические свойства, то применение их для сварочных работ, выполняемых по настоящему РД, не допускается.
4.12. Покрытые электроды после прокалки следует хранить в закрытых мешках из водонепроницаемой ткани (полиэтиленовая пленка) или в закрытой таре с крышкой с резиновым уплотнением или в сушильных шкафах при температуре не менее 50 °С, или в кладовых при температуре не ниже 18 °С и относительной влажностью воздуха не более 50 %. Срок хранения – согласно табл. 3.3 РД 558-97.
4.13.
Электроды выдаются в количестве,
необходимом для односменной работы
каждого сварщика, если не оговорены
более жесткие требования. При выдаче
должна проверяться марка электродов
по этикеткам или биркам, по окраске
торца.
Электроды на рабочем месте сварщика должны находиться в переносном ящике-пенале или термосе емкостью на одну-две пачки электродов и защищены от попадания на них воды, грязи, нефтепродуктов, источников огня.
4.14. Порядок учета, хранения, выдачи и возврата сварочных материалов устанавливается инструкцией производственной организации с учетом данных требований.
4.15. Для ручной аргонодуговой сварки в качестве неплавящегося электрода следует применять электроды из вольфрама марок ЭВЛ, ЭВИ-1, ЭВИ-2, ЭВИ-3, ЭВТ-15 по ГОСТ 23949-80, лантанированного вольфрама марки ВЛ по ТУ 48-19-27-77 или иттрированного вольфрама марки СВИ-1 по ТУ 48-19-221-83 диаметром 2-4 мм.
4.16.
Для аргонодуговой сварки в качестве
защитного газа следует применять аргон
высшего и первого сортов с физико-химическими
показателями по ГОСТ 10157-79. Допускается
использовать газообразный и жидкий
аргон. Ротаметры расхода газа следует
проверять в соответствии с ГОСТ 8122-74.
4.17. Рекомендуемое сварочное оборудование приведено в Приложении 6.
5. Аттестация технологии сварки
5.1. Аттестация технологии сварки выполняется в соответствии с РД 558-97.
5.2. Аттестация технологии сварки производится для каждой группы однотипных сварных соединений. Определение понятия однотипности приведено в п. 2.2 данного РД.
5.3. Результаты механических испытаний должны удовлетворять требованиям, приведенным в табл. 4
Таблица 4
Критерии качества при механических испытаниях сварных соединений
Вид испытаний | Критерии качества | |
Теплоустойчивые стали | Высоколегированные стали | |
1. | Равнопрочность основному металлу | |
2. Статический изгиб (корнем шва наружу, внутрь, на ребро) тип образцов XVII, XVIII ГОСТ 6996-66 | Угол загиба 50° при 20 мм, 40 при > 20 мм | Угол загиба 100° |
3. Сплющивание (для труб Dy<50 мм, S<4 мм), тип образцов XXX ГОСТ 6996-66 | Просвет “в” между сжимающими поверхностями при появлении первой трещины должен быть не более где и – наружный диаметр и толщина стенки | |
4. тип образцов VI ГОСТ 6996-66 | 49 при +20°С 39,2 при -45 °С (по требованию проектировщика) | 69 |
Влияние температуры отжига на реакционную активность выделения кислорода нанолистов оксида меди-кобальта
. 2021 8 марта; 11 (3): 657.
doi: 10.3390/nano11030657.
Гыль Хан Ким 1 2 , Парк Ю Сей 1 2 , Ючан Ян 1 , Мён Дже Чан 1 , Джехун Чжон 1 , Джи-Хун Ли 1 , Парк Хан-Сэм 3 , Ён Хо Парк 2 , Сун Мук Чой 1 , Джуён Ли 1
Принадлежности
- 1 Департамент энергетики и электронных материалов, Отдел поверхностных материалов, Корейский институт материаловедения, Чханвон 642831, Корея.

- 2 Факультет материаловедения и инженерии, Пусанский национальный университет, Пусан 46241, Корея.
- 3 IT&New Application Battery Development, LG Chem, Тэджон 34112, Корея.
- PMID: 33800286
- PMCID: PMC7998886
- DOI: 10.3390/нано11030657
Бесплатная статья ЧВК
Геул Хан Ким и др.
Наноматериалы (Базель). .
Бесплатная статья ЧВК
. 2021 8 марта; 11 (3): 657.
doi: 10.3390/nano11030657.
Авторы
Гыль Хан Ким 1 2 , Парк Ю Сей 1 2 , Ючан Ян 1 , Мён Дже Чан 1 , Джехун Чжон 1 , Джи-Хун Ли 1 , Парк Хан-Сэм 3 , Ён Хо Парк 2 , Сун Мук Чой 1 , Джуён Ли 1
Принадлежности
- 1 Департамент энергетики и электронных материалов, Отдел поверхностных материалов, Корейский институт материаловедения, Чангвон 642831, Корея.

- 2 Факультет материаловедения и инженерии, Пусанский национальный университет, Пусан 46241, Корея.
- 3 IT&New Application Battery Development, LG Chem, Тэджон 34112, Корея.
- PMID: 33800286
- PMCID: PMC7998886
- DOI: 10.3390/нано11030657
Абстрактный
Разработка высокоэффективных, очень стабильных и недорогих электродов для реакции выделения кислорода (OER) является сложной задачей в технологии электролиза воды. Однако катализаторы OER на основе Ir и Ru с высокой эффективностью OER трудно коммерциализировать в качестве катализаторов на основе драгоценных металлов. Поэтому необходимо исследование катализаторов ОЭР, замещенных неблагородными металлами и обладающих высокой активностью и стабильностью. В этом исследовании нанолистовой электрод из оксида меди-кобальта (CCO) был синтезирован путем электроосаждения гидроксида меди-кобальта (CCOH) на пене Ni с последующим отжигом. ССОН отжигали при различных температурах, и при температурах выше 250 °С структура изменялась на структуру ССО. Кроме того, было замечено, что нанолисты агломерируются при отжиге при 300 °C. Электрод CCO, отожженный при 250 ° C, имел большую площадь поверхности и эффективные пути электронной проводимости в результате прямого роста на пене Ni. Таким образом, приготовленный ССО-электрод проявлял повышенную активность ОЭР (1,6 В при 261 мА/см 2 ) по сравнению с CCOH (1,6 В при 144 мА/см 2 ), Co 3 O 4 (1,6 В при 39 мА/см 2 ) и коммерческим IrO 2 2 1,6 В при 14 мА/см 2 ) электроды.
Однако катализаторы OER на основе Ir и Ru с высокой эффективностью OER трудно коммерциализировать в качестве катализаторов на основе драгоценных металлов. Поэтому необходимо исследование катализаторов ОЭР, замещенных неблагородными металлами и обладающих высокой активностью и стабильностью. В этом исследовании нанолистовой электрод из оксида меди-кобальта (CCO) был синтезирован путем электроосаждения гидроксида меди-кобальта (CCOH) на пене Ni с последующим отжигом. ССОН отжигали при различных температурах, и при температурах выше 250 °С структура изменялась на структуру ССО. Кроме того, было замечено, что нанолисты агломерируются при отжиге при 300 °C. Электрод CCO, отожженный при 250 ° C, имел большую площадь поверхности и эффективные пути электронной проводимости в результате прямого роста на пене Ni. Таким образом, приготовленный ССО-электрод проявлял повышенную активность ОЭР (1,6 В при 261 мА/см 2 ) по сравнению с CCOH (1,6 В при 144 мА/см 2 ), Co 3 O 4 (1,6 В при 39 мА/см 2 ) и коммерческим IrO 2 2 1,6 В при 14 мА/см 2 ) электроды. Оптимизированный катализатор также продемонстрировал высокую активность и стабильность в условиях высокого pH, продемонстрировав свой потенциал в качестве недорогого и высокоэффективного электродного материала для OER.
Оптимизированный катализатор также продемонстрировал высокую активность и стабильность в условиях высокого pH, продемонстрировав свой потенциал в качестве недорогого и высокоэффективного электродного материала для OER.
Ключевые слова: электродные материалы; электроосаждение; катализ неблагородными металлами; реакция выделения кислорода; катализатор на основе оксида переходного металла; расщепление воды.
Заявление о конфликте интересов
Авторы заявляют об отсутствии конфликта интересов.
Цифры
Рисунок 1
Схематическое изображение катализатора CCO…
Рисунок 1
Схема приготовления катализатора CCO с использованием электроосаждения и термообработки при 200,…
Рисунок 1 Схематическое изображение приготовления катализатора CCO с использованием электроосаждения и термообработки при 200, 250 и 300 °C.
Рисунок 2
( а , б )…
Рисунок 2
( a , b ) СЭМ изображения и ( c ) XRD картина…
фигура 2( a , b ) СЭМ-изображения и ( c ) рентгенограмма электроосажденного CCOH. ( d ) Предлагаемая структура Cu 1-x Co x (OH) 2 (NO 3 ).
Рисунок 3
РЭМ-изображения, показывающие изменения…
Рисунок 3
РЭМ-изображения, показывающие изменения морфологии CCO в зависимости от температуры: ( a )…
Рисунок 3 СЭМ-изображений, демонстрирующих изменения морфологии CCO в зависимости от температуры: ( a ) 150, ( b ) 200, ( c ) 250 и ( d ) 300 °C соответственно.
Рисунок 4
Рентгенограммы CCO после…
Рисунок 4
Рентгенограммы ХСО после обработки при разных температурах: (сверху вниз)…
Рисунок 4Рентгенограммы ХСО после обработки при разных температурах: (сверху вниз) 150, 200, 250 и 300 °С.
Рисунок 5
( a ) ТЭМ высокого разрешения…
Рисунок 5
( a ) Изображение ПЭМ высокого разрешения (синий, CuO d (200) = 0,229 нм;…
Рисунок 5 ( a ) Изображение ПЭМ высокого разрешения (синий, CuO d (200) = 0,229 нм; красный, CCO d (133) = 0,187 нм и d (224) = 0,163 нм), ( b ) карты элементов ЭДС (по часовой стрелке) O, Co и Cu и ( c ) Co 2p и ( d ) Спектр уровня ядра Cu 2p XPS CCO-250 ° C.
Рисунок 6
( а , б )…
Рисунок 6
( a , b ) Кривые LSV (85% IR – компенсация) и ( c…
Рисунок 6( a , b ) Кривые LSV (85% IR – компенсация) и ( c ) перенапряжения при различных плотностях тока для катализаторов CCO (150, 200, 250 и 300 °C) в 1 M КОН при комнатной температуре. ( d ) графики Тафеля, ( e ) результаты EIS и ( f ) C dl катализаторов CCO (150, 200, 250 и 300 °C).
Рисунок 7
( a ) Кривая хронопотенциометрии…
Рисунок 7
( a ) Хронопотенциометрическая кривая CCO-250 °C при плотности тока…
Рисунок 7 ( a ) Хронопотенциометрическая кривая CCO-250 °C при плотности тока 20 мА см -2 в 1 М КОН в течение 100 ч. На вставке показано СЭМ-изображение морфологии поверхности CCO после испытания на долговечность. ( b ) Рентгенограммы, ( c ) Co 2p и ( d ) Cu 2p CCO-250 °C после испытаний на долговечность.
На вставке показано СЭМ-изображение морфологии поверхности CCO после испытания на долговечность. ( b ) Рентгенограммы, ( c ) Co 2p и ( d ) Cu 2p CCO-250 °C после испытаний на долговечность.
Рисунок 8
( a ) Кривые РТС…
Рисунок 8
( a ) Кривые РТС (85% IR -компенсированные) для CCO-250 °C в 1…
Рисунок 8 ( a ) Кривые LSV (85% IR – компенсация) для CCO-250 °C в 1 и 5 М KOH при комнатной температуре. ( b ) Хронопотенциометрическая кривая CCO (250 °C) при плотности тока 20 мА см -2 в 5 М КОН в течение 100 ч. ( c ) СЭМ-изображение, показывающее морфологию поверхности CCO (250 °C) после испытаний на долговечность.
См. это изображение и информацию об авторских правах в PMC
Похожие статьи
Электрохимически осажденный аморфный оксид меди, легированный кобальтом и никелем, как эффективный электрокатализатор реакции окисления воды.
Асгар М.А., Али А., Хайдер А., Захир М., Нисар Т., Вагнер В., Ахтер З. Асгар М.А. и соавт. АСУ Омега. 2021 июл 19;6(30):19419-19426. doi: 10.1021/acsomega.1c01251. Электронная коллекция 2021 3 августа. АСУ Омега. 2021. PMID: 34368529 Бесплатная статья ЧВК.
Электроосаждение пленок IrO 2 с большой площадью поверхности на войлоке Ti как эффективный катализатор реакции выделения кислорода.
Пак Й.Дж., Ли Дж., Пак Й.С., Ян Дж., Джанг М.
 Дж., Чон Дж., Чхве С., Ли Дж.В., Квон Дж.Д., Чой С.М.
Пак Ю.Дж. и др.
Фронт хим. 2020 23 окт;8:593272. doi: 10.3389/fchem.2020.593272. Электронная коллекция 2020.
Фронт хим. 2020.
PMID: 33195098
Бесплатная статья ЧВК.
Дж., Чон Дж., Чхве С., Ли Дж.В., Квон Дж.Д., Чой С.М.
Пак Ю.Дж. и др.
Фронт хим. 2020 23 окт;8:593272. doi: 10.3389/fchem.2020.593272. Электронная коллекция 2020.
Фронт хим. 2020.
PMID: 33195098
Бесплатная статья ЧВК.Бинарные оксигидроксидные нанолисты FeCo как высокоэффективные бифункциональные электрокатализаторы для полного расщепления воды.
Нгуен Т.Х., Ли Дж., Бэ Дж., Лим Б. Нгуен Т.Х. и соавт. Химия. 2018 26 марта; 24 (18): 4724-4728. doi: 10.1002/chem.201800022. Epub 2018 27 февраля. Химия. 2018. PMID: 29430737
3 D пористые нитриды никеля-кобальта, нанесенные на пену никеля, как эффективные электрокатализаторы для общего расщепления воды.
Ван И, Чжан Б, Пан В, Ма Х, Чжан Дж.
 Ван Ю и др.
ХимСусХим. 2017 9 ноября; 10 (21): 4170-4177. doi: 10.1002/cssc.201701456. Epub 2017 12 октября.
ХимСусХим. 2017.
PMID: 28857449
Ван Ю и др.
ХимСусХим. 2017 9 ноября; 10 (21): 4170-4177. doi: 10.1002/cssc.201701456. Epub 2017 12 октября.
ХимСусХим. 2017.
PMID: 28857449Взаимодействия катализатора и носителя, способствующие кислому электрохимическому катализу выделения кислорода: мини-обзор.
Луо З., Ван Дж., Чжоу В., Ли Дж. Луо Зи и др. Молекулы. 2023 28 февраля; 28 (5): 2262. doi: 10,3390/молекулы28052262. Молекулы. 2023. PMID: 368 Бесплатная статья ЧВК. Обзор.
Посмотреть все похожие статьи
Цитируется
Перестраиваемый перенос носителя полимерного нитрида углерода с проводящим заряд CoV 2 O 6 ∙2H 2 O для фотокатализатора O 2 Эволюция.

Цзан С., Цай С., Чен М., Тэн Д., Цзин Ф., Ленг З., Чжоу И., Линь Ф. Занг С. и др. Наноматериалы (Базель). 2022 5 июня; 12 (11): 1931. doi: 10.3390/nano12111931. Наноматериалы (Базель). 2022. PMID: 35683786 Бесплатная статья ЧВК.
Тонкие пленки оксидов металлов и полупроводников P-типа: синтез и применение в химических датчиках.
Мумен А, Кумараге GCW, Комини Э. Мумен А. и др. Датчики (Базель). 2022 10 февраля; 22 (4): 1359. дои: 10.3390/s22041359. Датчики (Базель). 2022. PMID: 35214257 Бесплатная статья ЧВК. Обзор.
Рекомендации
- Pu Z., Luo Y., Asiri AM, Sun X. Эффективное электрохимическое расщепление воды, катализируемое электроосажденной пленкой на основе наночастиц диселенида никеля.
 Приложение ACS Матер. Интерфейсы. 2016; 8: 4718–4723. дои: 10.1021/acsami.5b12143.
–
DOI
–
пабмед
Приложение ACS Матер. Интерфейсы. 2016; 8: 4718–4723. дои: 10.1021/acsami.5b12143.
–
DOI
–
пабмед
- Pu Z., Luo Y., Asiri AM, Sun X. Эффективное электрохимическое расщепление воды, катализируемое электроосажденной пленкой на основе наночастиц диселенида никеля.
- Куай Л., Гэн Дж., Чен С., Кан Э., Лю Ю., Ван К., Генг Б. Надежный подход с помощью аэрозольного распыления к производству и оптимизации катализаторов на основе аморфных оксидов металлов для электрохимического расщепления воды. Ангью. хим. Междунар. Эд. 2014;53:7547–7551. doi: 10.1002/anie.201404208. – DOI – пабмед
- Лю Г.
 , Йе С., Ян П., Сюн Ф., Фу П., Ван З., Чен З., Ши Дж., Ли К. Обеспечение интегрированного фотоанода из нитрида тантала для приближения к теоретическому пределу фототока для солнечной воды расщепление. Энергетическая среда. науч. 2016;9:1327–1334. DOI: 10.1039/C5EE03802B.
–
DOI
, Йе С., Ян П., Сюн Ф., Фу П., Ван З., Чен З., Ши Дж., Ли К. Обеспечение интегрированного фотоанода из нитрида тантала для приближения к теоретическому пределу фототока для солнечной воды расщепление. Энергетическая среда. науч. 2016;9:1327–1334. DOI: 10.1039/C5EE03802B.
–
DOI
- Лю Г.
- Бхатт М.Д., Ли Дж.С. Недавний теоретический прогресс в разработке фотоанодных материалов для солнечных фотоэлектрохимических элементов, расщепляющих воду. Дж. Матер. хим. А. 2015;3:10632–10659. DOI: 10.1039/C5TA00257E. – DOI
- Ван Дж.
 , Юэ С., Ян Ю., Сирисомбунчай С., Ван П., Ма С., Абудула А., Гуан Г. Обильные в земле бифункциональные катализаторы на основе переходных металлов для общего электрохимического расщепления воды: обзор. J. Alloys Compd. 2020;819:153346. doi: 10.1016/j.jallcom.2019.153346.
–
DOI
, Юэ С., Ян Ю., Сирисомбунчай С., Ван П., Ма С., Абудула А., Гуан Г. Обильные в земле бифункциональные катализаторы на основе переходных металлов для общего электрохимического расщепления воды: обзор. J. Alloys Compd. 2020;819:153346. doi: 10.1016/j.jallcom.2019.153346.
–
DOI
- Ван Дж.
Грантовая поддержка
- 2019M3E6A106367513/Национальный исследовательский фонд Кореи
- PNK7550/Корейский институт материаловедения
Влияние температуры отжига на реакционную активность при выделении кислорода нанолистов оксида меди-кобальта Приложение ACS Матер. Интерфейсы. 2016; 8: 4718–4723. doi: 10.1021/acsami.5b12143. [PubMed] [CrossRef] [Академия Google]
2. Kuai L., Geng J., Chen C., Kan E., Liu Y., Wang Q., Geng B. Надежный подход с помощью аэрозольного распыления для производства и оптимизации катализаторов на основе аморфных оксидов металлов для электрохимической воды Разделение. Ангью. хим. Междунар. Эд. 2014;53:7547–7551. doi: 10.1002/anie.201404208. [PubMed] [CrossRef] [Google Scholar]
Kuai L., Geng J., Chen C., Kan E., Liu Y., Wang Q., Geng B. Надежный подход с помощью аэрозольного распыления для производства и оптимизации катализаторов на основе аморфных оксидов металлов для электрохимической воды Разделение. Ангью. хим. Междунар. Эд. 2014;53:7547–7551. doi: 10.1002/anie.201404208. [PubMed] [CrossRef] [Google Scholar]
3. Liu G., Ye S., Yan P., Xiong F., Fu P., Wang Z., Chen Z., Shi J., Li C. Enabling встроенный фотоанод из нитрида тантала, чтобы приблизиться к теоретическому пределу фототока для расщепления солнечной воды. Энергетическая среда. науч. 2016;9: 1327–1334. doi: 10.1039/C5EE03802B. [CrossRef] [Google Scholar]
4. Бхатт М.Д., Ли Дж.С. Недавний теоретический прогресс в разработке фотоанодных материалов для солнечных фотоэлектрохимических элементов, расщепляющих воду. Дж. Матер. хим. А. 2015;3:10632–10659. doi: 10.1039/C5TA00257E. [CrossRef] [Google Scholar]
5. Wang J., Yue X., Yang Y., Sirisomboonchai S., Wang P., Ma X., Abudula A. , Guan G. Обильные в земле на основе переходных металлов. бифункциональные катализаторы общего электрохимического расщепления воды: обзор. J. Alloys Compd. 2020;819:153346. doi: 10.1016/j.jallcom.2019.153346. [CrossRef] [Google Scholar]
, Guan G. Обильные в земле на основе переходных металлов. бифункциональные катализаторы общего электрохимического расщепления воды: обзор. J. Alloys Compd. 2020;819:153346. doi: 10.1016/j.jallcom.2019.153346. [CrossRef] [Google Scholar]
6. Wu X., Zhu C., Wang L., Guo S., Zhang Y., Li H., Huang H., Liu Y., Tang J., Kang Z. Стратегия управления двух-/четырехэлектронным путем расщепления воды мультидопированными катализаторами на основе углерода. Катал. 2017;7:1637–1645. doi: 10.1021/acscatal.6b03244. [CrossRef] [Google Scholar]
7. Liu J., Liu Y., Liu N., Han Y., Zhang X., Huang H., Lifshitz Y., Lee ST., Zhong J., Kang Z. Metal -свободный эффективный фотокатализатор для стабильного видимого расщепления воды по двухэлектронному пути. Наука. 2015;347:6225. doi: 10.1126/science.aaa3145. [PubMed] [CrossRef] [Академия Google]
8. Черевко С., Гейгер С., Касьян О., Кулик Н., Гроте Ж.-П., Саван А., Шреста Б.Р., Мерзликин С., Брейтбах Б., Людвиг А. и др. Реакции выделения кислорода и водорода на тонкопленочных электродах Ru, RuO 2 , Ir, IrO 2 в кислых и щелочных электролитах: сравнительное исследование активности и стабильности. Катал. Сегодня. 2016; 262:170–180. doi: 10.1016/j.cattod.2015.08.014. [CrossRef] [Google Scholar]
Катал. Сегодня. 2016; 262:170–180. doi: 10.1016/j.cattod.2015.08.014. [CrossRef] [Google Scholar]
9. Audichon T., Mayousse E., Morisset S., Morais C., Comminges C., Napporn T.W., Kokoh K.B. Электроактивность RuO 2 -IrO 2 смешанные нанокатализаторы для реакции выделения кислорода в водном электролизере, питаемом солнечным профилем. Междунар. Дж. Водородная энергия. 2014;39:16785–16796. doi: 10.1016/j.ijhydene.2014.07.170. [CrossRef] [Google Scholar]
10. Sahoo S., Rout CS Facile Электрохимический синтез пористых марганцево-кобальтовых сульфидов на основе тройных сульфидов переходных металлов Архитектуры для высокопроизводительных приложений хранения энергии. Электрохим. Акта. 2016;220:57–66. doi: 10.1016/j.electacta.2016.10.043. [Перекрестная ссылка] [Академия Google]
11. Пуркар В., Рэдицою В., Рэдицою А., Радули Ф.М., Манеа Р., Фроне А., Анастасеску М., Испас Г.К., Кэпреску С. Двухслойные покрытия на основе кремнеземных материалов и фталоцианина железа (III)— Сенсибилизированный фотокатализатор TiO2. Матер. Рез. Бык. 2021;138:111222. doi: 10.1016/j.materresbull.2021.111222. [CrossRef] [Google Scholar]
Матер. Рез. Бык. 2021;138:111222. doi: 10.1016/j.materresbull.2021.111222. [CrossRef] [Google Scholar]
12. Ма Б., Ян З., Чен Ю., Юань З. Фосфид кобальта Никель с трехмерной наноструктурой как высокоэффективный электрокатализатор для реакции выделения водорода как в кислых, так и в щелочных электролитах. Нано рез. 2019;12:375–380. doi: 10.1007/s12274-018-2226-2. [CrossRef] [Google Scholar]
13. Ходабахши М., Чен С., Е Т., Ву Х., Ян Л., Чжан В., Чанг Х. Иерархические сильно морщинистые триметаллические нанолисты фосфида NiFeCu на нанодендрите Ni3S2/Ni Пена как эффективный электрокатализатор реакции выделения кислорода. Приложение ACS Матер. Интерфейсы. 2020;12:36268–36276. doi: 10.1021/acsami.0c11732. [PubMed] [CrossRef] [Google Scholar]
14. Сабатини М.Т., Боултон Л.Т., Шеппард Т.Д. Боратный эфир: простые катализаторы для устойчивого синтеза сложных амидов. науч. Доп. 2017;3:e1701028. doi: 10.1126/sciadv.1701028. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
15. Jiang W.J., Niu S., Tang T., Zhang Q.H., Liu X.Z., Zhang Y., Chen Y.Y., Li J.H., Gu L., Wan L.J., et al. Модулированная кристалличностью электрокаталитическая активность тонкого слоя бората никеля(II) на Ni -3- B для эффективного окисления воды. Ангью. хим. Междунар. Эд. 2017;56:6572–6577. doi: 10.1002/anie.201703183. [PubMed] [CrossRef] [Google Scholar]
Jiang W.J., Niu S., Tang T., Zhang Q.H., Liu X.Z., Zhang Y., Chen Y.Y., Li J.H., Gu L., Wan L.J., et al. Модулированная кристалличностью электрокаталитическая активность тонкого слоя бората никеля(II) на Ni -3- B для эффективного окисления воды. Ангью. хим. Междунар. Эд. 2017;56:6572–6577. doi: 10.1002/anie.201703183. [PubMed] [CrossRef] [Google Scholar]
16. Bai B., Arandiyan H., Li J. Сравнение эффективности окисления формальдегида на нано-Co 3 O 4 , катализаторы 2D-Co 3 O 4 и 3D-Co 3 O 4 . заявл. Катал. Б. 2013; 142–143:677–683. doi: 10.1016/j.apcatb.2013.05.056. [CrossRef] [Google Scholar]
17. Ma C., Wang D., Xue W., Dou B., Wang H., Hao Z. Исследование окисления формальдегида на Co 3 O 4 -CeO 2 и Au/Co 3 O 4 -CeO 2 Катализаторы при комнатной температуре: эффективное удаление и определение механизма реакции. Окружающая среда. науч. Технол. 2011;45:3628–3634. doi: 10.1021/es104146v. [PubMed] [CrossRef] [Академия Google]
Окружающая среда. науч. Технол. 2011;45:3628–3634. doi: 10.1021/es104146v. [PubMed] [CrossRef] [Академия Google]
18. Дэнчилэ А.М., Кэпреску С., Бобирица С., Пуркар В., Гэрляну Г., Василе Э., Модроган С., Борда С., Доброта Д. Оптимизация технологических параметров получения композитов на основе Zn-Ti для повышения эффективности удаления H 2 S из синтез-газа. Процессы. 2020;8:562. doi: 10.3390/pr8050562. [CrossRef] [Google Scholar]
19. Пуркар В., Рэдитойу В., Николае К.А., Фроне А.Н., Рэдитойу А., Радулы Ф.М., Сомоги Р., Габор Р.А., Кэпреску С. Синтез и морфоструктурные свойства TiO 2 – материалы на основе. Дж. Оптоэлектрон. Доп. Матер. 2019;21:281–286. [Google Scholar]
20. Purcar V., Şomoghi R., Niţu S.G., Nicolae C.A., Alexandrescu E., Gîfu I.C., Gabor A.R., Stroescu H., Ianchiş R., Căprărescu S., et al. Влияние различных связующих агентов на материалы Nano-ZnO, полученные с помощью золь-гелевого процесса. Наноматериалы. 2017;7:439. doi: 10. 3390/nano7120439. [Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
3390/nano7120439. [Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
21. Purcar V., Cinteza O., Donescu D., Bala D., Ghiurea M., Petcu C., Caprarescu S. Модификация поверхности кремнезема частицы, которым помогает CO 2 . Дж. Суперкрит. Жидкости. 2014;87:34–39. doi: 10.1016/j.supflu.2013.12.025. [CrossRef] [Google Scholar]
22. Чой В.С., Чан М.Дж., Пак Ю.С., Ли К.Х., Ли Дж.Ю., Сео М.Х., Чой С.М. Трехмерные сотоподобные Cu 0,81 Co 2,19 O 4 Массивы нанолистов, поддерживаемые пеной Ni, и их высокая эффективность в качестве электродов выделения кислорода. Приложение ACS Матер. Интерфейсы. 2018;10:38663–38668. doi: 10.1021/acsami.8b12478. [PubMed] [CrossRef] [Академия Google]
23. Park H., Park B.H., Choi J., Kim S., Kim T., Youn Y.S., Son N., Kim J.H., Kang M. Улучшенные электрохимические свойства и характеристики OER путем замены Cu в NiCo 2 O 4 Структура шпинели. Наноматериалы. 2020;10:1727. doi: 10.3390/nano10091727. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
doi: 10.3390/nano10091727. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
24. Урсуа А., Барриос Э.Л., Паскуаль Дж., Мартин И.С., Санчис П. Интеграция коммерческих электролизеров щелочной воды с возобновляемыми источниками энергии: ограничения и улучшения. Междунар. Дж. Водородная энергия. 2016;41:12852–12861. doi: 10.1016/j.ijhydene.2016.06.071. [Перекрестная ссылка] [Академия Google]
25. Шаленбах М., Касьян О., Майрхофер К.Дж.Дж. Щелочной водный электролизер с никелевыми электродами обеспечивает эффективную работу при высокой плотности тока. Междунар. Дж. Водородная энергия. 2018;43:11932–11938. doi: 10.1016/j.ijhydene.2018.04.219. [CrossRef] [Google Scholar]
26. Миллер Х.А., Бузек К., Хнат Дж., Лоос С., Бернекер К.И., Вайсгарбер Т., Рёнч Л., Мейер-Хаак Дж. Зеленый водород из электролиза воды с анионообменной мембраной : Обзор последних разработок в области критических материалов и условий эксплуатации. Поддерживать. Энергетическое топливо. 2020;4:2114–2133. дои: 10.1039/C9SE01240K. [CrossRef] [Google Scholar]
дои: 10.1039/C9SE01240K. [CrossRef] [Google Scholar]
27. Andronescu C., Seisel S., Wilde P., Barwe S., Masa J., Chen Y.T., Ventosa E., Schuhmann W. Влияние температуры и концентрации электролита на структуру и каталитическая активность по выделению кислорода никель-железослоистого двойного гидроксида. хим. Евро. Дж. 2018; 24:13773–13777. doi: 10.1002/chem.201803165. [PubMed] [CrossRef] [Google Scholar]
28. Liu Y., Liang X., Gu L., Zhang Y., Li G.D., Zou X., Chen J.S. Коррозионная инженерия для эффективных электродов выделения кислорода со стабильной каталитической активностью в течение более 6000 часов. Нац. коммун. 2018;9:2609. doi: 10.1038/s41467-018-05019-5. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
29. Ли Дж., Ли Х., Лим Б. Химическое превращение нанолистов алкоксида железа в наночастицы FeOOH для высокоактивных и стабильных электрокатализаторов выделения кислорода. J. Ind. Eng. хим. 2018;58:100–104. doi: 10.1016/j.jiec.2017.09.013. [CrossRef] [Google Scholar]
30. Guo C.X., Li C.M. Формируемый при комнатной температуре гидроксид никеля, легированный железом, на пеноникелевой основе в качестве трехмерного электрода для выделения кислорода с низкой поляризацией и высокой плотностью тока. хим. коммун. 2018;54:3262–3265. дои: 10.1039/C8CC00701B. [PubMed] [CrossRef] [Google Scholar]
Guo C.X., Li C.M. Формируемый при комнатной температуре гидроксид никеля, легированный железом, на пеноникелевой основе в качестве трехмерного электрода для выделения кислорода с низкой поляризацией и высокой плотностью тока. хим. коммун. 2018;54:3262–3265. дои: 10.1039/C8CC00701B. [PubMed] [CrossRef] [Google Scholar]
31. Maiti U.N., Lim J., Lee K.E., Lee W.J., Kim S.O. Трехмерная форма, межфазное гелеобразование восстановленного оксида графена для высокопроизводительных суперконденсаторов большой емкости. Доп. Матер. 2014;26:615–619. doi: 10.1002/adma.201303503. [PubMed] [CrossRef] [Google Scholar]
32. Ю Л., Рен З. Систематическое изучение влияния компенсации iR на электролиз воды. Матер. Сегодня физ. 2020;14:100253. doi: 10.1016/j.mtphys.2020.100253. [Перекрестная ссылка] [Академия Google]
33. Джалал М.Р., Ходжати Х., Джалал Дж.Р., Эбрахими С., Бигхаши М.Р.З. Синтез микролистов гидроксида меди (Cu 2 (OH) 3 NO 3 ) путем плазменного электролиза водного раствора Cu(NO 3 ) 2 в атмосферном воздухе. J. Интерфейсы Тонкие пленки Низкие размеры. Сист. ДЖИТЛ. 2018;1:109–112. [Google Scholar]
J. Интерфейсы Тонкие пленки Низкие размеры. Сист. ДЖИТЛ. 2018;1:109–112. [Google Scholar]
34. Wang X., Huang L. Новый одностадийный метод синтеза наноколец гидроксида нитрата меди. Транс. Цветные металлы. соц. Китай. 2009 г.;19:с480–с484. doi: 10.1016/S1003-6326(10)60093-3. [CrossRef] [Google Scholar]
35. Кальяни М., Эмерсон Р.Н. Электроосаждение нанокристаллического оксида кобальта на пористом медном электроде для суперконденсатора. Дж. Матер. науч. Матер. Электрон. 2019;30:1214–1226. doi: 10.1007/s10854-018-0389-y. [CrossRef] [Google Scholar]
36. Xia H., Peng Z., Cuncail V., Zhao Y., Hao J., Huang Z. Самоподдерживающиеся пористые нанопроволоки из оксида кобальта с улучшенными электрокаталитическими характеристиками в отношении реакции выделения кислорода. Дж. Хим. науч. 2016;128:1879–1885. doi: 10.1007/s12039-016-1192-z. [CrossRef] [Google Scholar]
37. Chi B., Lin H., Li J. Распределение катионов Cu x Co 3−x O 4 и его электрокаталитическая активность в реакции выделения кислорода. Междунар. Дж. Гидрог. Энергия. 2008; 33: 4763–4768. doi: 10.1016/j.ijhydene.2008.05.032. [CrossRef] [Google Scholar]
Междунар. Дж. Гидрог. Энергия. 2008; 33: 4763–4768. doi: 10.1016/j.ijhydene.2008.05.032. [CrossRef] [Google Scholar]
38. Чжан Б., Цзян К., Ван Х., Ху С. Индуцированная фтором динамическая самореконструкция поверхности приводит к неожиданно эффективному катализатору выделения кислорода. Нано Летт. 2019;19:530–537. doi: 10.1021/acs.nanolett.8b04466. [PubMed] [CrossRef] [Google Scholar]
39. Liu K., Zhang C., Sun Y., Zhang G., Shen X., Zou F., Zhang H., Wu Z., Wegener E.C., Taubert C.J. и др. Высокоэффективный катализатор из сплава фосфида переходного металла для реакции выделения кислорода. АКС Нано. 2018;12:158–167. doi: 10.1021/acsnano.7b04646. [PubMed] [CrossRef] [Google Scholar]
40. Hai G., Jia X., Zhang K., Liu X., Wu Z., Wang G. Высокоэффективный катализатор выделения кислорода с использованием двумерного ультратонкого металла. органические каркасы нанолисты. Нано Энергия. 2018;44:345–352. doi: 10.1016/j.nanoen.2017.11.071. [Перекрестная ссылка] [Академия Google]
41. Xu H., Wang B., Shan C., Xi P., Liu W., Tang Y. Двойной гидроксид NiFe, легированный Ce, ультратонкие нанолисты/наноуглеродный иерархический нанокомпозит как эффективный катализатор выделения кислорода. Приложение ACS Матер. Интерфейсы. 2018;10:6336–6345. doi: 10.1021/acsami.7b17939. [PubMed] [CrossRef] [Google Scholar]
Xu H., Wang B., Shan C., Xi P., Liu W., Tang Y. Двойной гидроксид NiFe, легированный Ce, ультратонкие нанолисты/наноуглеродный иерархический нанокомпозит как эффективный катализатор выделения кислорода. Приложение ACS Матер. Интерфейсы. 2018;10:6336–6345. doi: 10.1021/acsami.7b17939. [PubMed] [CrossRef] [Google Scholar]
42. Ван Ю., Ван С., Лю Д., Чжоу Л., Ду Р., Ли Т.Т., Мяо Т., Цянь Дж., Ху Ю., Хуан S. Изготовление на месте обернутых графеном наноцветов CuO, полученных из MOF, с помощью нормального импульсного напряжения для окисления воды. хим. коммун. 2020;56:8750–8753. дои: 10.1039/D0CC03132A. [PubMed] [CrossRef] [Google Scholar]
43. Бай Л., Хсу К.С., Александр Д.Т.Л., Чен Х.М., Ху С. Двухатомный катализатор кобальт-железо для реакции выделения кислорода. Варенье. хим. соц. 2019;141:14190–14199. doi: 10.1021/jacs.9b05268. [PubMed] [CrossRef] [Google Scholar]
44. Stern L.A., Feng L., Song F., Hu X. Ni 2 P как катализатор Януса для расщепления воды: активность выделения кислорода Ni 2 Наночастицы Р. Энергия. Окружающая среда. науч. 2015;8:2347–2351. дои: 10.1039/C5EE01155H. [CrossRef] [Google Scholar]
Энергия. Окружающая среда. науч. 2015;8:2347–2351. дои: 10.1039/C5EE01155H. [CrossRef] [Google Scholar]
45. Бабар П.Т., Локханде А.С., Павар Б.С., Ганг М.Г., Джо Э., Го С., Сурьяванши М.П., Павар С.М., Ким Дж.Х. Оценка электрокаталитических характеристик тонких пленок гидроксида и оксида кобальта для реакции выделения кислорода. заявл. Серф. науч. 2018; 427: 253–259. doi: 10.1016/j.apsusc.2017.07.142. [CrossRef] [Google Scholar]
46. Dang W.J., Shen Y.Q., Lin M., Jiao H., Xu L., Wang Z.L. Электрокатализатор, не содержащий благородных металлов, на основе смешанного металлоорганического каркаса CoNi для реакции выделения кислорода. J. Alloys Compd. 2019;792:69–76. doi: 10.1016/j.jallcom.2019.03.399. [CrossRef] [Google Scholar]
47. Hu Q., Li G., Liu X., Zhu B., Li G., Fan L., Chai X., Zhang Q., Liu J., He C. Сочетание наночастиц пентландита и углеродных сетей с двойным легированием для получения эффективных и стабильных электрокатализаторов для окисления кислой воды. Дж. Матер. хим. А. 2019;7:461–468. doi: 10.1039/C8TA09534E. [CrossRef] [Google Scholar]
Дж. Матер. хим. А. 2019;7:461–468. doi: 10.1039/C8TA09534E. [CrossRef] [Google Scholar]
48. Wang F., Xue H., Tian Z., Xing W., Feng L. Fe 2 P в качестве нового эффективного катализатора-промотора в системе Pd/C для электролиза муравьиной кислоты. – реакция окисления в топливных элементах. J. Источник питания. 2018; 375:37–42. doi: 10.1016/j.jpowsour.2017.11.055. [Перекрестная ссылка] [Академия Google]
49. Zhang W., Qi J., Liu K., Cao R. Интегрированный электрод на основе никеля из стратегии аутологичного роста для высокоэффективного окисления воды. Доп. Энергия Матер. 2016;6:1502489. doi: 10.1002/aenm.201502489. [CrossRef] [Google Scholar]
50. Gao M., Sheng W., Zhuang Z., Fang Q., Gu S., Jing J., Yan Y. Эффективное окисление воды с использованием наноструктурированного α-гидроксида никеля в качестве Электрокатализатор. Варенье. хим. соц. 2014; 136:7077–7084. doi: 10.1021/ja502128j. [PubMed] [CrossRef] [Академия Google]
51. Andronescu C., Barwe S.



 Растяжение, тип образцов VII, VIII ГОСТ
6996-66
Растяжение, тип образцов VII, VIII ГОСТ
6996-66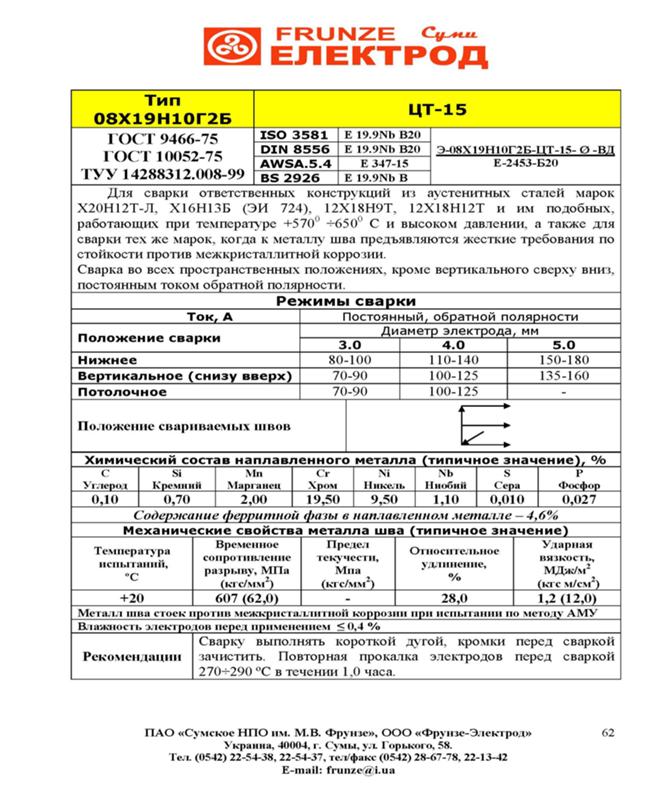 Ударная вязкость (Дж/см
),
Ударная вязкость (Дж/см
),

 Дж., Чон Дж., Чхве С., Ли Дж.В., Квон Дж.Д., Чой С.М.
Пак Ю.Дж. и др.
Фронт хим. 2020 23 окт;8:593272. doi: 10.3389/fchem.2020.593272. Электронная коллекция 2020.
Фронт хим. 2020.
PMID: 33195098
Бесплатная статья ЧВК.
Дж., Чон Дж., Чхве С., Ли Дж.В., Квон Дж.Д., Чой С.М.
Пак Ю.Дж. и др.
Фронт хим. 2020 23 окт;8:593272. doi: 10.3389/fchem.2020.593272. Электронная коллекция 2020.
Фронт хим. 2020.
PMID: 33195098
Бесплатная статья ЧВК. Ван Ю и др.
ХимСусХим. 2017 9 ноября; 10 (21): 4170-4177. doi: 10.1002/cssc.201701456. Epub 2017 12 октября.
ХимСусХим. 2017.
PMID: 28857449
Ван Ю и др.
ХимСусХим. 2017 9 ноября; 10 (21): 4170-4177. doi: 10.1002/cssc.201701456. Epub 2017 12 октября.
ХимСусХим. 2017.
PMID: 28857449
 Приложение ACS Матер. Интерфейсы. 2016; 8: 4718–4723. дои: 10.1021/acsami.5b12143.
–
DOI
–
пабмед
Приложение ACS Матер. Интерфейсы. 2016; 8: 4718–4723. дои: 10.1021/acsami.5b12143.
–
DOI
–
пабмед , Йе С., Ян П., Сюн Ф., Фу П., Ван З., Чен З., Ши Дж., Ли К. Обеспечение интегрированного фотоанода из нитрида тантала для приближения к теоретическому пределу фототока для солнечной воды расщепление. Энергетическая среда. науч. 2016;9:1327–1334. DOI: 10.1039/C5EE03802B.
–
DOI
, Йе С., Ян П., Сюн Ф., Фу П., Ван З., Чен З., Ши Дж., Ли К. Обеспечение интегрированного фотоанода из нитрида тантала для приближения к теоретическому пределу фототока для солнечной воды расщепление. Энергетическая среда. науч. 2016;9:1327–1334. DOI: 10.1039/C5EE03802B.
–
DOI , Юэ С., Ян Ю., Сирисомбунчай С., Ван П., Ма С., Абудула А., Гуан Г. Обильные в земле бифункциональные катализаторы на основе переходных металлов для общего электрохимического расщепления воды: обзор. J. Alloys Compd. 2020;819:153346. doi: 10.1016/j.jallcom.2019.153346.
–
DOI
, Юэ С., Ян Ю., Сирисомбунчай С., Ван П., Ма С., Абудула А., Гуан Г. Обильные в земле бифункциональные катализаторы на основе переходных металлов для общего электрохимического расщепления воды: обзор. J. Alloys Compd. 2020;819:153346. doi: 10.1016/j.jallcom.2019.153346.
–
DOI